연구 목표
면역세포치료사업단은 생물의약품 중 다양한 종류의 항암 T 세포치료제 개발 및 비임상연구를 수행하고 있으며, 현재국립암센터에서 자체적으로 수행중인 자가유래 항암 T 세포치료제의 임상시험 승인신청 및 임상시험 수행을 지원하고 있습니다.
연구 사업의 필요성
국립암센터는 지난 10년간 난치성 암환자에게 새로운 치료기회를 제공하기 위해 항암면역세포치료제인 T 세포치료제의 개발 및 임상시험 수행하였습니다.
지난 7년간의 항암 T 세포치료제 연구개발 및 임상시험를 통해 인체를 구성하는 암단백질을 표적하는 T 세포치료제만으로는 제한적인 환자만이 완치 가능함을 확인하였습니다.
T 세포치료제의 완치율을 향상하기 위해서는 T 세포치료제의 생체내 기능을 높일 수 있는 병용요법의 개발이 필요하며, 또한 살아있는 치료제 특성으로 인해 현재의 진단방법으로는 면역치료의 예후예측이 불가능하므로 새로운 예후예측 방법의 개발이 필요합니다.
최근 노바티스사의 유전자세포치료제인 CD19 CAR (Chimeric Ag Receptor) T 세포치료제 (Kymriah)의 미국 시판 허가 (2017.11)로 인해 항암제 시장의 새로운 기원이 열리고 있습니다.
* 유전자세포치료제인 CD19 CAR-T는 급성림프구성 백혈병 (ALL) 환자에서 획기적인 치료 효과(완치율 25% → 90%로 상승)를 증명함으로써 암 치료의 새로운 기원을 열고 있습니다.
Kymriah의 높은 완치율과 가격 ($75만)으로 인해 새로운 T 세포치료제의 개발 및 제품화에 대한 관심이 급증하고 있으며, 이러한 현상이 지속될 경우 고가의 치료비용으로 인해 건강보험 체계에도 악영향이 미칠 것이므로, 꾸준한 국내 연구개발이 필요합니다.
연구 사업
- 항암 T 세포치료제 개발 및 임상시험
- - 림프종, 뇌종양, 고형암 치료제 제1상 임상시험 식약처 승인 및 림프종 치료제 제1상 임상시험 완료(‘15. 12)하였고,
- ㈜유틸렉스에 선급기술료 33억원을 받고 면역세포치료제 기술이전(‘16. 3)을 하였습니다.
< 국립암센터 항암 T 세포치료제 주요성과 >
- 앱비앤티셀(림프종 치료용) 제1상 임상시험 종료(‘11. 4 - ’15.12) 및 논문 게재(‘16. 4)
- 위티앤티셀(뇌종양 치료용) 제1상 임상시험 식약처 승인(‘12. 12)
- 터티앤티셀(폐, 위, 췌장, 간암 등 고형암치료용) 제1상 임상시험 식약처 승인(‘14. 3)
- 앱비앤티셀, 터터앤티셀, 위티앤티셀 등 면역세포 치료제 기술이전(‘16. 3)
연구 분야
- 항암 T 세포치료제 생산을 위한 플랫폼 개발: 암항원 특이적 CD8 T 세포를 선택적으로 분리/증식할 수 있는 제조공정 개발 및 개량 (http://www.youtube.com/watch?v=_mN2pZ5TZA0)
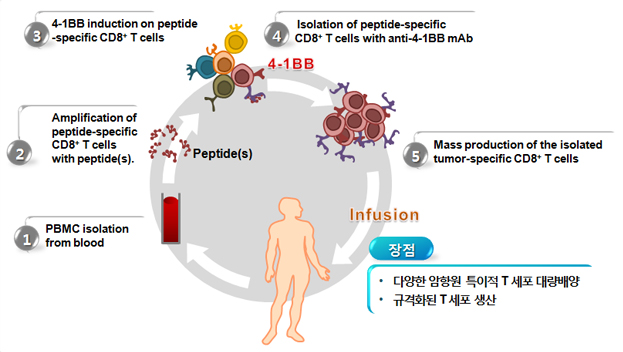
- 자가유래 항암 T 세포치료제의 개발: 각종 암의 대표적인 암항원을 표적으로 항암 T 세포치료제를 지속적으로 개발하여 임상시험 수행
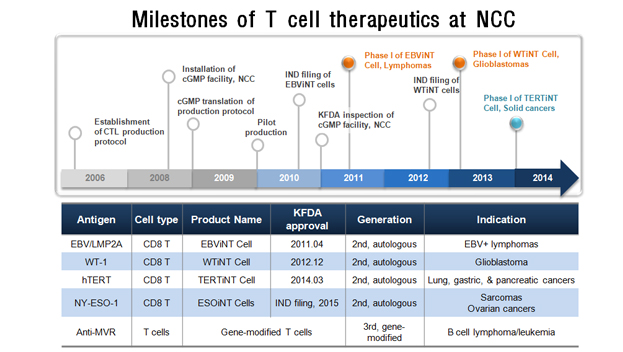
- 2006 Establishment of CTL production protocol
- 2008 Installation of cGMP facility, NCC
- 2009 cGMP translation of production protocol
- 2010 Pilot production
- 2010 IND filing of EBVINT cells
- 2011 KFDA inspection of CGMP facility, NCC
- 2011 Phase I of EBViNT Cell, Lymphomas
- 2012 IND filing of WTiNT cells
- 2013 Phase I of WTiNT Cel Glioblastomas
- 2014 Phase I of TERTiNT Cell, Solid cancers
Milestones of T cell therapeutics at NCC Antigen Cell type Product Name KFDA approval Generation Indication EBV/LMP2A CD8 T EBVINT Cell 2011.04 2nd, autologous EBV+ lymphomas WT-1 CD8 T WTINT Cell 2012.12 2nd, autologous Glioblastoma hTERT CD8 T TERTINT Cell 2014.03 2nd, autologous Lung, gastric, & pancreatic cancers NY-ESO-1 CD8 T ESOINT Cells IND fling, 2015 2nd, autologous Sarcomas Ovarian cancers Anti-MVR T cells Gene-modified T cells 3rd, gene-modified B cell lymphoma/leukemia - Gene-modified T 세포치료제의 개발
- 일정한 규격의 T 세포치료제를 빠른 시간내에 배양하기 위해서, 유전자 조작을 통해 T 세포에 항원 특이성을 부여하는 방법들이 오랫동안 연구개발되었습다. 1) 특정암항원을 인식하는 TCRa/b 유전자를 확보하여 이들 유전자를 activated T cell에 lentiviral virus를 이용하여 도입하는 형태의 TCR-engineered T 세포, 2) 특정 항원을 인식하는 항체의 scFv를 T cell activation domain과 결합시켜 T 세포에 도입시킨 형태의 chimeric Ag receptor (CAR) T cell, 3) TCR 유전자에 T cell activation domain을 결합시켜 T 세포에 도입함으로써 항원 특이성과 빠른 증식을 유도하는 방식의 chimeric TCR T 세포치료제 등이 그 대표적인 예입니다.
CAR T cell은 세포표면항원을 인식하는 특성을 가지고 있어 강력한 효력을 나타내지만, 부작용을 최소화 하기 위해서는 일반 조직에 발현되지 않는 세포표면 암항원을표적해야 하므로 개발이 어렵다는 단점을 가지고 있습니다. 이에 비해 TCR-engineered T cell 또는 chimeric TCR T cell은 세포내 항원을 표적하므로, 비교적 안전하다는 장점이 있지만 HLA type에 따른 많은 TCR 유전자를 확보해야만 하는 단점을 가지고 있습니다. 또한 gene-modified T 세포치료제는 T 세포내로유전자를 도입하기 위해 retrovirus 또는 lentivirus와 같은 고가의 바이러스를 사용해야 하므로, 유전자 조작을 하지 않은 natural T 세포치료제에 비해 상당히 높은 생산비용을 필요로 합니다.
본 사업단은 제조방법 개량, TCRa/b 유전자 확보, 새로운 항체 개발등을 통해 다양한 방식으로 gene-modified T 세포치료제의 개발을 수행함으로써, 안전하고 효과적인 T 세포치료제를 적은 비용으로 생산할 수 있는 방법을 개발하고 있습니다.
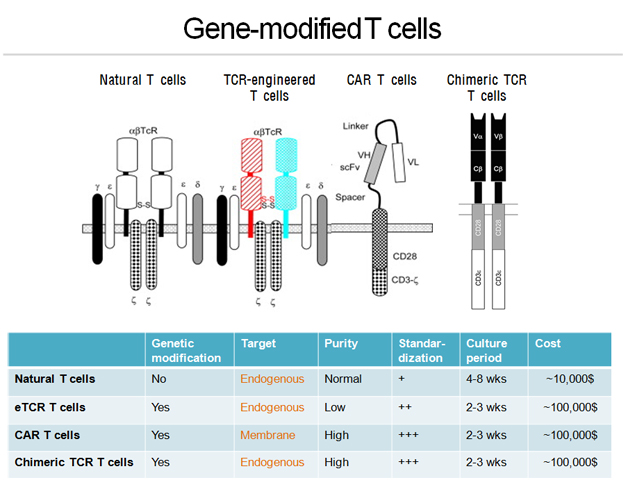
Gene-modified T cells Genetic modification Target Purity Standardization Culture period Cost Natural T cells No Endogenous Normal + 4-8 wks ~ 10,000$ eTCR T cells Yes Endogenous Normal ++ 2-3 wks ~ 100,000$ CAR T cells Yes Membrane Normal +++ 2-3 wks ~ 100,000$ Chimeric TCR T cells Yes Endogenous Normal +++ 2-3 wks ~ 100,000$
최종 수정일 : 2017.12.19